2019中国医药审批关键词:创新药预计超40款 生物类似药时代开启
2019年已然步入尾声,回首2019年,许多进展值得深入思考,如:1. 首款生物类似药汉利康获批上市,中国进入生物类似药时代;2. 一致性评价进展显著,一致性评价后的集采扩面;3. 新版《药品注册管理办法(征求意见稿)》公布,《突破性治疗药物工作程序》和《优先审评审批工作程序》发布;4. 医保目录和医保谈判全部完成,降价降价降价成为一个关键词;5. 诺西那生钠、度拉糖肽、司库奇尤单抗、地舒单抗、达雷妥尤单抗、贝利尤单抗等39款创新药获批,其中进口药物33款,6款国产药品。
本文将首先关注创新药和生物类似药的审评审批情况。2018-2019两年,国家药品监督管理局批准药物的数量在大幅增加,新药获批数量均超40款。截止2019年12月05日,NMPA在2019年已经批准39款创新药上市,同时,阿斯利康PD-L1单抗Durvalumab和百济神州PD-1单抗替雷利珠单抗技术审评完成,已经开始行政审批,预计2019年年底均会获批上市。
生物类似药方面,中国生物类似药以汉利康 (利妥昔单抗)为始,格乐立(阿达木单抗),贝伐珠单抗 (QL1101) 等等多个生物类似药均将在2019年先后获批上市,毫无疑问,2019年是中国生物类似药元年。
一.审评在明显提速:临床急需新药正在加速药物中国上市进程
严谨的笔者,必须用数字说话!
2017年,2018年,2019年中国国家药品监督管理局均批准了约40款创新药物上市,这明显加速了药物的中国上市进程。
以2019年数据为例:
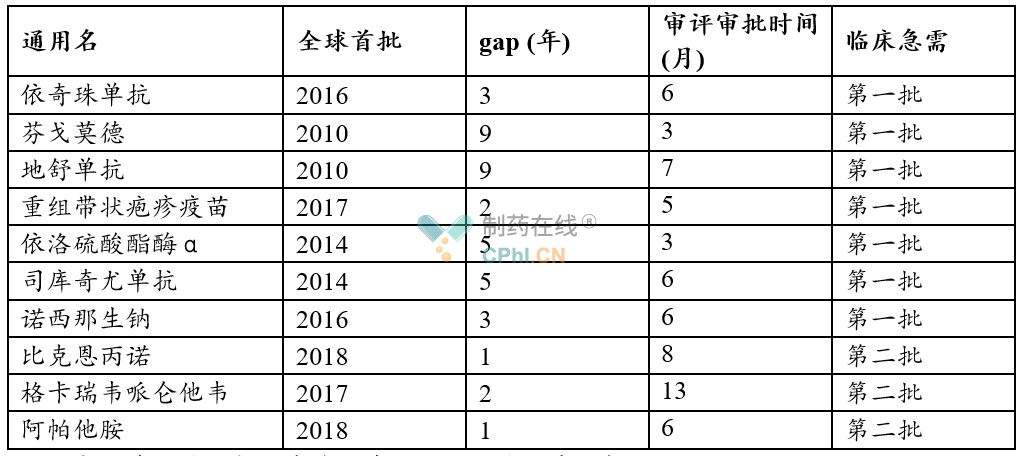
gap:中国获批时间与全球首次获批之间的时间差,年
从2018年,2019年药物获批上市数据来看,临床急需境外新药名单的确在加速进口创新药的国内上市进程。特别的,从2019年看,纳入临床急需药物,1. 药物中国审评审批周期普遍 < 6个月,这在2018年之前,是无法想象的,尤其是诺西那生钠这类罕见病药物;2.同时,药物中国可及性在改善,全球新药物中国获批时间差在缩短,纳入临床急需境外新药,这个gap平均为4年;3. 2019年获批,未纳入临床急需的,这个gap约为6.44年。
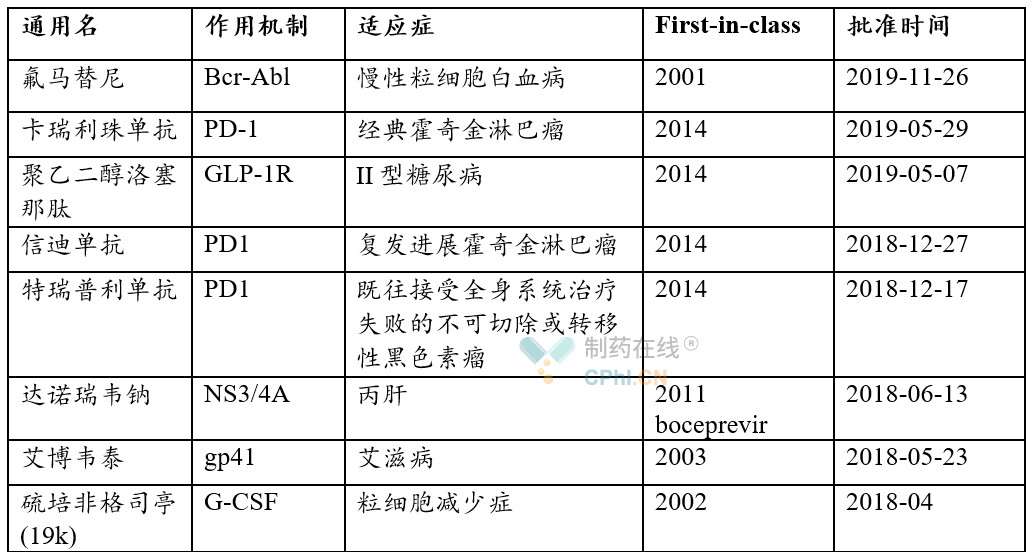
二.中国创新药:仍缺乏真正意义上的first-in-class
截至目前,2019年国家药品监督管理局已获批上市的创新药中,进口药33款,6款国产药品。然后,获批上市的6款药物中,仍无first-in-class,特瑞普利单抗为代表的PD-1单抗可算是fast-follower!!!
三.2019年进口药:多个first-in-class| best-in-class进入中国
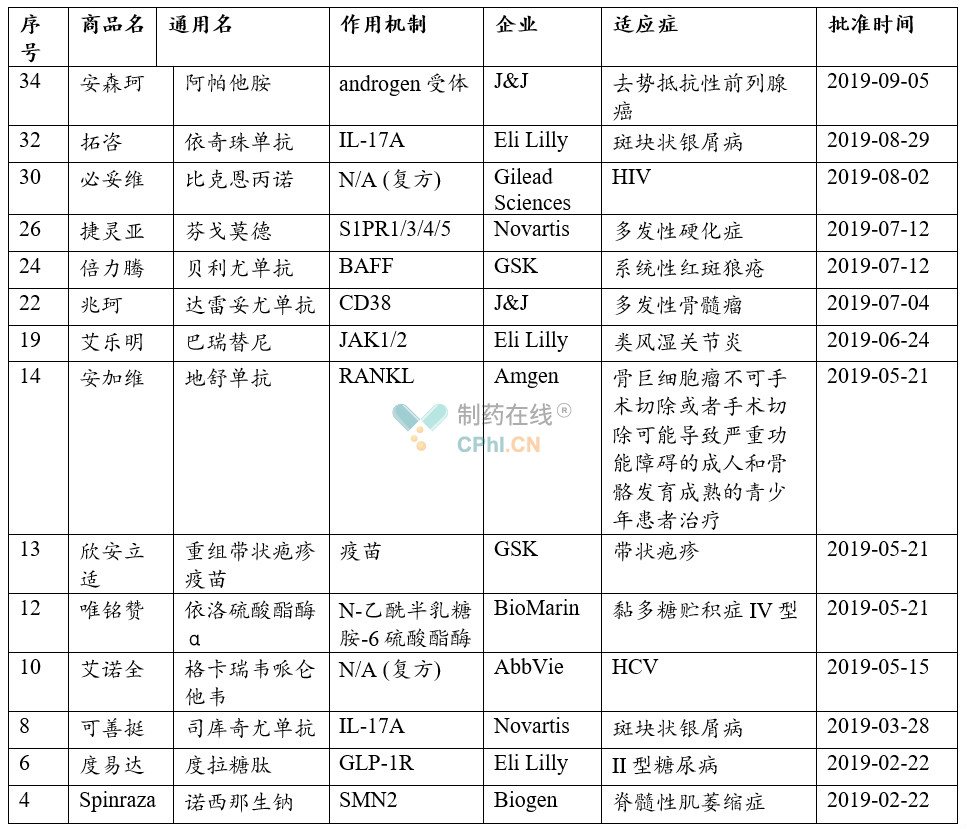
33款进口药物中,得益于近年罕见病药物和临床急需境外新药审评审批改革的推进,
1. 诺西那生钠、依洛硫酸酯酶α、重组带状疱疹疫苗、芬戈莫德等罕见病药物快速进入中国,可及性明显改善,这是具有重大意义的;
2. 丙肝、艾滋病best-in-class药物中国获批上市,2018年-2019年,中国快速获批上市了多款丙肝DAA药物,艾滋病TAF, 整合酶抑制剂STR方案,其中,丙肝best-in-class艾诺全,艾滋病单一片剂best-in-class必妥维中国已获批;
3. 糖尿病畅销药物度易达中国获批上市,目前,GLP-1R激动剂度易达仍是全球最畅销的一款超级重磅炸 弹;
4. 贝利尤单抗是全球首个BAFF人源化IgG2λ单克隆抗体,现有SLE治疗选择不多,贝利尤单抗联合标准治疗法用于治疗自身抗体阳性的成人活动性SLE患者具有良好的获益风险比。这是一个突破;
5. 银屑病、类风湿关节炎重磅药物司库奇尤单抗、依奇珠单抗、巴瑞替尼获批。2017年以来,中国国内自身免疫疾病重磅创新治疗药物的可及性已经大大改善,IL-12/23单抗,IL-17单抗,JAK类药物国内已获批,药物竞争格局正在发生剧变。
6. 多发性骨髓瘤治疗药物也在快速可及,伊沙佐米、达雷妥尤单抗国内可及。
重要进口药品一览
四:生物类似药元年:中国正式进入生物类似药时代
2019年02月,生物类似药汉利康 (利妥昔单抗) 获批上市,第一个严格按照《生物类似药研发与评价技术指导原则(试行)》获批的药物,汉利康的开发和商业化见证了中国生物类似药产业的发展。生物类似药的获批上市助力药物可及,1398元/100mg:10ml,相比原研大幅降价!
目前,国内生物类似药神评审批进展总结为下表;
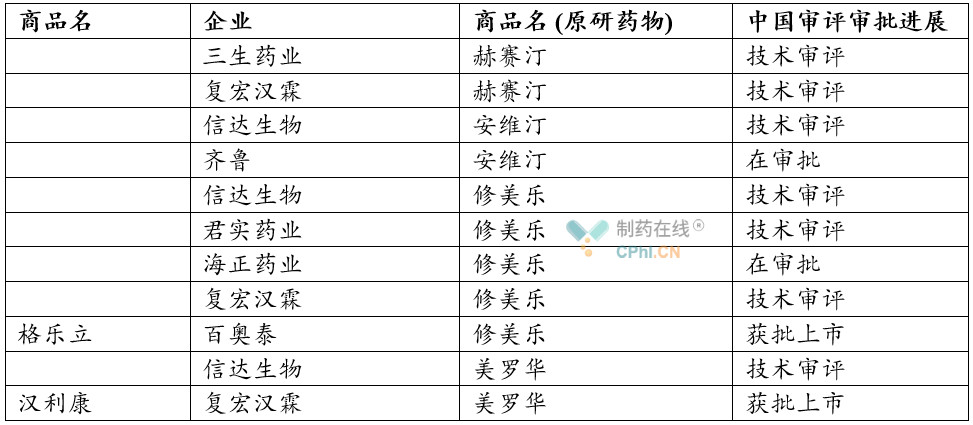
截至目前,利妥昔单抗生物类似药1款获批、1款上市技术审评;阿达木单抗生物类似药1款获批上市,1款行政审批,3款技术审评;贝伐珠单抗生物类似药1款启动行政审批,1款技术审评中;曲妥珠单抗生物类似药2款均处于技术审评中。
2020年,中国生物类似药至少会达到11款,生物类似药时代将蓬勃发展。
本文中,主要介绍2019年创新药和生物类似药审评审批,2020年,国内创新药审评审批仍有很多期待,如国产重磅创新药物泰它西普,安进重磅双抗Blincyto,恒瑞氟唑帕利等!
重磅创新药物中国快速获批上市背后是政策改革的大力推进,下文笔者将会从2019年重要政策和医保为着眼点,回顾2019年重磅政策!
作者简介:1°C,医药行业从业人员,希望自己的专业文字会越来越有温度,医药知识能够服务更多人,打破信息知识的壁垒!

